摘要
含铜不锈钢已被证明是有效的降低细菌感染的风险。然而,其抗菌机制仍存在争议。因此,选取3种不同Cu含量的430铁素体不锈钢,从材料和生物学两方面,通过灭活细菌的方式进行更深入的研究。其中,电化学和抗菌实验结果表明,Cu含量的增加同时提高了430不锈钢的耐腐蚀性能和抗菌性能。此外,还发现大肠杆菌(大肠杆菌)对430含cu不锈钢的表面具有快速灭活的能力。x射线光电子能谱(XPS)辅助离子螯合实验证明,铜(I)比铜(II)在接触杀伤效率中起着更重要的作用,导致活性氧(ROS)产生更多。
图形抽象

摘要
含铜不锈钢已被证实能够有效地降低细菌感染所带来的风险。然而, 关于其抗菌机制仍存在争议。因此, 我们选择3种不同铜含量的430铁素体不锈钢, 通过细菌灭活的方法, 从材料学和生物学两个方面进行深入的研究。电化学和抗菌实验结果表明, 铜含量的增加同时提高了430不锈钢的耐蚀性能和抗菌性能。此外, 通过干法接种技术发现大肠杆菌在430含铜不锈钢表面可以快速的被灭活。XPS结合离子螯合实验证明,由于铜(I)可以促进产生更多的活性氧(ROS),因此在接触杀灭过程中铜(I)比铜(II)起着更为重要的作用。
简介
近年来,COVID-19、SARS、禽流感等一些重大公共卫生事件与微生物污染密切相关,严重威胁人类健康,甚至严重影响国家和全球经济建设的发展[1,2].众所周知大肠杆菌(大肠杆菌)可引致严重的细菌感染,经常出现在开放性伤口[3.,4].其中,细菌生物膜的形成通常会增强细菌对抗生素的耐药性,使用抗生素是治疗细菌感染的一种常用方法。此外,大肠杆菌由于其传染性强,广泛存在于日常生活环境中,也会引起其他人类疾病[5].因此,开发结构与功能一体化的抗菌材料特别是抗菌金属材料具有重要的意义。铜也是众多生物不可缺少的微量元素和重要的杀菌元素[6,7].含铜不锈钢已被证明具有广谱抗菌性能和优良的机械性能,这是由于铜在钢中添加了固有的抗菌活性[8,9,10,11].值得注意的是,430铁素体不锈钢由于其良好的加工性能、抗应力腐蚀性能和较低的成本,被广泛用于洗衣机滚筒、室内面板和厨房设施[12,13,14,15].因此,在430铁素体不锈钢中添加Cu有望改善材料的抗菌性能,进一步拓宽其应用领域。
然而,近年来关于含铜不锈钢抗菌机理的研究结果仍存在争议。传统观点认为不锈钢中富Cu沉淀产生的Cu离子的释放是主要的抗菌机制[16,17,18].然而,更矛盾的是,铜离子的释放浓度远低于最低抑制浓度(MIC)。最近,张等[19]发现细菌与含铜马氏体不锈钢表面的直接接触程度调控着细菌的杀菌过程。然而,对于含铜铁素体不锈钢,其抗菌机理的研究还不够。
在这项工作中,含铜铁素体不锈钢的抗菌效率大肠杆菌从接触杀伤的角度进行研究。重点研究了金属表面铜离子的价态和活性氧(ROS)水平,探讨了含铜铁素体不锈钢的抗菌机理。研究结果将有助于促进抗菌不锈钢的进一步发展。
实验
标本的材料和制备
实验用的430不锈钢(SS)和430- cu SS试样尺寸为10 mm × 10 mm × 5 mm,由太钢(太原钢铁(集团)有限公司提供。表格1列出他们的作品。试样在800°C溶液处理30 min,然后空气淬火。随后,为了在430-Cu SS中获得富cu沉淀,试样在550℃时效60 min,然后空气淬火[20.].最终,试样依次用碳化硅纸(SiC)从150到1000粒度进行研磨。在接下来的实验中,用75%乙醇在超声波浴中消毒20分钟,然后用紫外灯照射20分钟,以规范表面条件。
电化学测量
在3.5% NaCl溶液中进行了开路电位(OCP)、动电位极化(PD)和电化学阻抗谱(EIS)测试,评价了实验钢的耐蚀性。使用恒电位器/恒电位器(Reference 600TM, Gamry Instruments, Inc., USA),三电极电池,在24°C下进行这些实验。其中,试样作为工作电极,接触面积为1 cm2采用硅橡胶密封,避免缝隙腐蚀。采用饱和甘汞电极(SCE)和铂电极(PE)分别作为参比电极和对电极。OCP操作时间为3600 s,以保持样品的化学稳定性。然后,测量频率为0.01 ~ 100,000 Hz,振幅为5 mV的正弦信号,评价钝化膜的耐蚀性,并通过ZSimpWin 3.10软件得到相应值。PD扫描速率为0.33 mV·s−1电势从−0.5到2.0 V南加州爱迪生公司同时对含铜430钢与合同钢的耐腐蚀性能进行了比较。每个样品至少测试三次,以确保上述测量的重现性。
菌种及培养基
本研究中革兰氏阴性菌ATCC25922 (大肠杆菌)购自广东省微生物研究所微生物培养物收集中心。取pH = 7.2±0.2的Luria-Bertani (LB)培养基,在37℃相对湿度为70%的湿度热槽中培养上述菌株24 h。取由NaCl (5.0 g)、蛋白胨(10.0 g)、牛肉提取物(5.0 g)、琼脂(20.0 g)和蒸馏水(1 L)组成的牛肉提取物蛋白胨培养基为细菌生存提供营养物质,调整培养基pH为7.2 ~ 7.4。实验前,所有实验室用品在121℃高压蒸汽灭菌锅中灭菌20分钟。
抗菌活性
采用平板计数法评价实验材料的抗菌性能[21].首先用紫外分光光度计(752 N, INESA)测量波长为600 nm的菌悬液的光密度(OD)浓度,然后用PBS溶液从初始的1 × 10连续稀释菌悬液8到1 × 103.菌落形成单位(CFU)·ml−1.为保证菌悬液在标本表面得到良好的铺展,将标本置于24孔板中,接种菌浓度为1 × 10的菌悬液50 μl6CFU·毫升−1在37℃,相对湿度为70%的条件下孵育24 h。然后将接种后的标本放入各含2.5 ml PBS的离心管中,用涡旋振荡器振荡40 s。将振荡后的菌悬液100 μl滴于琼脂平板上,与牛肉提取物蛋白胨培养基共培养24 h。抗菌率计算公式如下:
在哪里一个表示抗菌率,一个CG为430 SS表面的菌落数量,和一个如为430-Cu SS表面细菌菌落数,每个样品至少重复3次实验。
材料表面接触压痕的测量
采用相同菌落形成单元(CFU)的干镀和湿镀两种方法对含铜430铁素体不锈钢的接触杀灭机理进行了研究。5 μl菌悬液,浓度为~ 1 × 107CFU·毫升−1细菌悬液50 μl,浓度约为1 × 106CFU·毫升−1分别用于干镀和湿镀研究。之前在平板计数法中描述了其他详细的操作步骤。
SEM形貌观察
利用扫描电子显微镜(SEM,日立,S-3400 N)和偶联背散射电子探测器观察细菌在材料表面粘附的形态。将材料表面的菌悬液用PBS溶液冲洗三次。然后标本在2.5%戊二醛中4℃浸泡4 h,分别用不同浓度(50%、60%、70%、80%、90%、95%、100%)的1 ml乙醇依次脱水20 min,使生物膜固定在材料表面[22,23].最后,在室温(22±2)℃)下干燥24 h,并喷涂导电金涂层。
生活/死染色
采用活/死染色法,live/dead®BacLight TM细菌活力试剂盒(L7012,美国)检测生物活性/灭活细菌,并评估其对材料表面的膜损伤。试剂盒含红色碘化丙啶(PI)染色剂和绿色SYTO-9染色剂两种核酸染色剂。首先去除材料表面接种的菌悬液,用PBS溶液冲洗三次。用20 μl试剂盒(SYTO-9/PI)和1ml PBS在37℃潮湿黑暗的环境中染色20 min。标本干燥后立即转移到微载玻片上,共聚焦激光扫描显微镜(CLSM, MTC-600,美国)观察。其中,PI穿透的受损膜呈现514 nm的荧光红色,SYTO-9穿透的完整膜呈现488 nm的荧光绿色[24].此外,CLSM的操作是在黑暗的环境中进行的。使用NIS-Elements Viewer软件捕捉三维图像。
铜离子螯合分析
用浓度为5 mmol·L的bathocuproine disulfonic acid (BCS)螯合430-Cu SS表面的Cu (I)和Cu (II)−1乙二胺四乙酸(EDTA),浓度为10 mmol·L−1分别为(25].将含PBS溶液和含有螯合剂的不同溶液的菌悬液用干镀法分别接种于标本表面40、80和120 min,最后通过计算抑菌率来确定结果。
XPS测试
利用ESCALAB 250(美国热真空发生器)表面分析系统进行x射线光电子能谱(XPS),进一步分析430-Cu SS表面的化学成分和元素价。材料表面采用单色源(激发能量为1486.6 eV的Al Kα线),来自150w的双Mg/Al阳极。分析仪与样品夹角保持在90º,蚀刻速率为0.1 nm·s−1.采用XPS峰软件进行光谱分析。
ROS的确定
ROS检测试剂盒(Beyotime,中国)检测细胞内ROS大肠杆菌在材料表面[26].孵化后大肠杆菌2 h后用PBS轻轻冲洗2次,再用含10 μmol·L的PBS 1 ml−1将2 ',7 ' -二氯二氢荧光素二乙酸酯(DCFH-DA)加到标本上,在37°C潮湿黑暗的环境中共培养30 min,同时加入含50 mg·ml的PBS (1ml)−1阳性对照组加入Rosup。最后,采用激发波长为488 nm,发射波长为525 nm的CLSM对荧光图像进行捕获。
结果与讨论
电化学特性
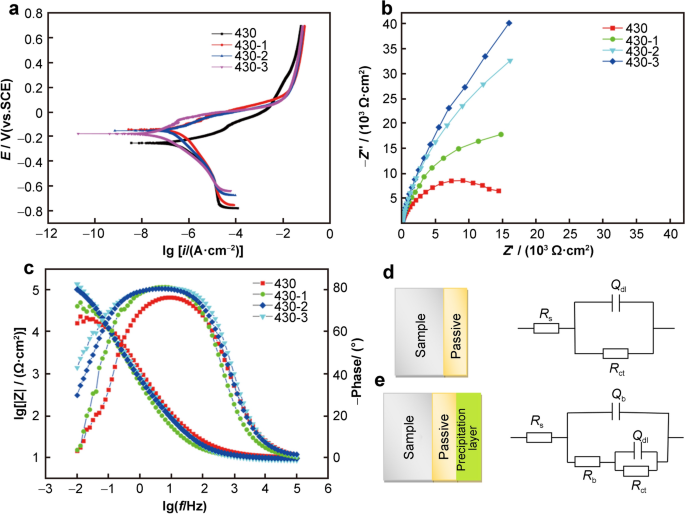
数字1a为不同Cu含量430-Cu SS的动态电位极化曲线;相应的电化学参数包括腐蚀电流密度(我相关系数)和腐蚀电位(E相关系数)由Gamry Echem Analyst™软件安装,如表所示2.一般来说,我相关系数而且E相关系数数值能反映材料的耐腐蚀性能。一个更小的我相关系数表明腐蚀速率较低,耐腐蚀性能较好,而E相关系数表示腐蚀反应的热力学趋势,且较大E相关系数意味着更高的耐腐蚀性[27,28].数字1A清楚地表明E相关系数430-Cu SS的含量随Cu含量的增加呈增加趋势我相关系数430-Cu SS的变化趋势相反。同时,表中的数据2确认430-Cu的SS相对较低E相关系数和更高的我相关系数,表明其腐蚀倾向比普通的430 SS要弱。特别是当Cu含量达到1.94%时,其腐蚀倾向明显减弱我相关系数最小值为0.0705 μA·cm−2,而我相关系数430 SS的耐蚀性是430 - 3 SS的4.8倍,说明Cu的加入在很大程度上提高了430 SS的耐蚀性。
耐蚀性提高的原因可能是在430-Cu SS表面形成了致密稳定的钝化膜[29,30.].钝化膜主要由金属氧化物组成,通过阻断电子的传递降低电化学反应速率,有效防止腐蚀反应物和高渗透性离子的侵入[31,32].数字1b、c为EIS分析得到的430-Cu SS的Nyquist图和Bode图,其中Z”,Z″表示阻抗|的实部和虚部Z|,f分别表示阻抗幅值和频率。一般来说,在Nyquist图中,圆弧半径越大,极化电阻越大,腐蚀速率越低[33,34].如图所示。1b,在430 SS中随着Cu含量的增加,电容弧逐渐增大,说明Cu的加入对腐蚀反应的发生起到了至关重要的抑制作用。如图所示。1c,波德图显示了阻抗随Cu含量逐渐增加的趋势,峰值相位角略有增加。此外,还可以发现430 SS和430-1 SS的相位角图都呈现出一个对称的相位角峰;因此,它只包含一个时间常数。而430-2和430-3的SS在中低频范围(< 10 Hz)出现了一个宽的不对称峰,显示了至少两个倍常数的叠加。为了进一步量化EIS数据,利用ZSimpwin®软件生成等效电路(EEC),并结合物理模型R年代(问pRp),R年代(问pRp(问戴斯。莱纳姆:Rct))(图1d、e)及拟合物性参数如表所示2.其中,R年代是溶液阻力,Rp是铜的耐腐蚀产物的沉积膜和钝化膜,Rct为电荷转移电阻,问p而且问戴斯。莱纳姆:分别表示钝化膜和电双层的电容。在表2,溶液抗性无明显差异。总电阻(Rt)可以反映材料的腐蚀行为。如表所示2, Cu的加入明显提高了430ss的极化电阻,表明其耐蚀性增强。
抗菌性能
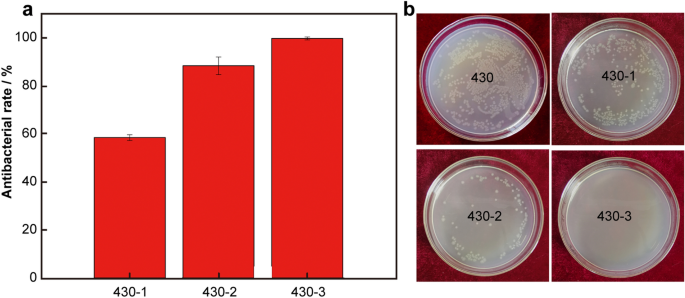
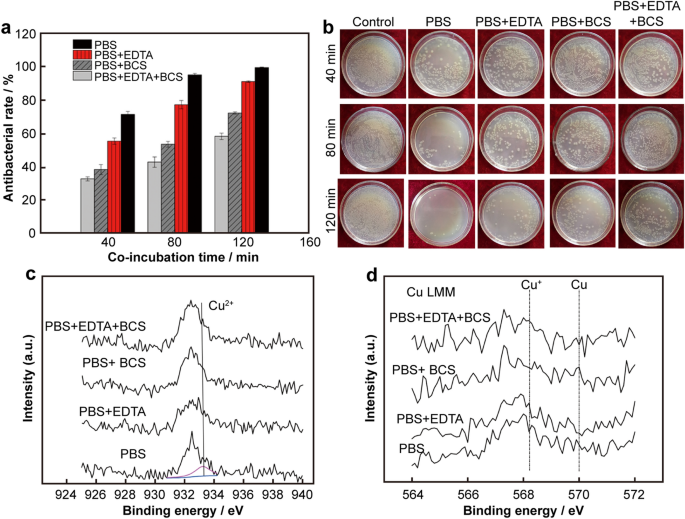
数字2A表示抗菌率(一个)对实验不锈钢的影响大肠杆菌,对应的代表性菌落图像如图所示。2b.从图中可以看出。2a、b表明随着Cu含量从0.99%增加到1.94%,430-Cu SS的抑菌率从最初的~ 60%明显提高到99.9%,表现出一定的抑菌活性。这是因为Cu含量越高,富Cu沉淀的体积分数越高,有利于Cu离子从SS表面释放,最终表现出良好的抗菌性能。
增强抗菌效果的干镀法
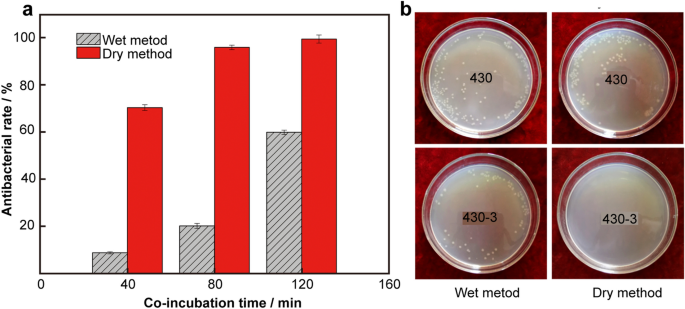
前期实验证实,Cu含量对430-Cu SS的抗菌性能有重要影响,但前期研究发现,释放的Cu离子浓度远低于Cu离子对其的最低抑菌浓度大肠杆菌.因此,铜离子从含铜SS表面的释放作为主要的抗菌机制是有争议的。相反,近年来接触性死亡的机制受到了更多的关注[35,36,37,38].本研究采用干接种和湿接种两种方法来调节细菌与430-Cu SS的接触程度,如图所示。3.一、干法和湿法在短时间内抗菌性能有显著差异。采用干镀法,数量多大肠杆菌接种40 min后,材料表面菌落显著减少。430-Cu SS接种2 h后的抑菌率大肠杆菌高达99%。如图所示。3.B,培养皿上几乎没有细菌菌落。相比之下,有很多大肠杆菌湿法接种2 h后检测菌落,抑菌率仅为58.97%。总之,在固定接种时间下,干燥法测定的抑菌效果始终高于湿法。与湿接种相比,干接种时细菌与430-Cu SS表面的接触更加直接和连续,接种时间的延长进一步促进了细菌与Cu离子的直接接触和释放,大大提高了430-Cu SS的抗菌效率。
材料表面抗菌性能可视化
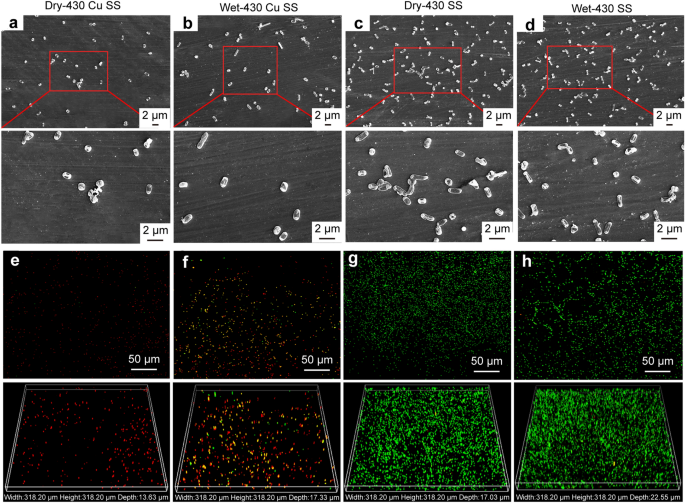
为了进一步阐述430-Cu SS的抗菌性能,采用活/死染色技术结合扫描电镜观察材料表面细菌的形态[39].数字4a-d为大肠杆菌分别用干法和湿法接种2 h后贴于材料表面。干燥法处理的430-Cu SS表面只发现零星的菌体,形态呈皱缩或裂纹状,如图所示。4a.作为比较,绝大多数的大肠杆菌在430ss表面附着了棒状和丰富的形状,如图所示。4c.然而,与干燥法相比,大肠杆菌无论材料为430-Cu SS,湿法接种均具有较好的活性条件(图;4b)或430 SS(图。4d).以上结果表明,430 SS无明显的抑菌活性,但430- cu SS具有优良的抑菌性能大肠杆菌在干孕育的条件下是有效的。数字4e-h显示的CLSM图像大肠杆菌分别用干法和湿法接种2 h的试样表面。SYTO-9将所有细胞膜完好和受损的细菌细胞的DNA都染成绿色,而PI只能将细胞膜受损细胞的DNA染成红色[40].430ss表面分布着大量的绿点,表明其膜大肠杆菌与430ss接触后整合。而430-Cu SS表面出现大量的红点,说明430-Cu SS有效地破坏了膜结构大肠杆菌.
不同价态铜离子的影响
本研究利用螯合剂BCS和EDTA分别在430-Cu SS表面螯合Cu (I)和Cu (II)离子,以阐明不同价态Cu离子在430-Cu SS表面接触杀伤行为中的作用。如图所示。5a, b, 430-Cu SS螯合表面的抗菌率显著降低,其中添加EDTA的抗菌率高于添加BCS。当添加两种螯合剂时,抑菌活性最低。此外,随着孵育时间的增加,抑菌率的提高表明,螯合剂的加入对其自然繁殖有一定的保护作用大肠杆菌.此外,铜(I)螯合时这种保护作用更明显,表明铜(I)在接触杀伤效率中起着更重要的毒性作用大肠杆菌比铜(II)。
以期进一步阐明铜价态对其杀菌能力的影响大肠杆菌,利用XPS分析了430-Cu SS共孵育后表面不同价态Cu的分布大肠杆菌添加不同螯合剂2h5c为溅射20 s后的XPS谱,其中Cu、Cu (I)和Cu (II)的特征峰分别在结合能为932.6、932.5和933.5 eV处分化[41].XPSPEAK得到430-Cu SS表面相应的Cu (II)含量,其中A、B、C和D溶液中Cu (II)的含量分别为0.69 %、2.26 %、1.19 %和2.37 %。随着螯合剂用量的增加,Cu (II)的含量明显增加,尤其是EDTA的加入,明显增加了Cu (II)的含量。这是因为Cu (II)与EDTA反应迅速,形成Cu (II)-EDTA络合物,限制了Cu (II)向Cu (I)的歧化反应;因此,大部分Cu (I)最终会留在430-Cu SS的表面,同样,BCS的加入也会与Cu (I)直接络合形成Cu (I)-BCS2,导致Cu (I)的失效完全转化为Cu (II),导致Cu (II)含量略有增加。
但是由于在XPS光谱中Cu和Cu (I)的结合能非常接近,很难准确区分Cu和Cu (I),因此我们采用Cu LMM的俄格谱结合XPS谱来准确区分Cu和Cu (I)。如图所示。5d、主峰和卫星峰分别约位于570 eV和568 eV处。根据相关文献,Cu和Cu (I)的LMM特征峰分别位于570 eV和568 eV左右[42].因此,Cu LMM光谱证实了Cu和Cu (I)在430-Cu SS表面的存在,并且随着螯合剂的加入,Cu和Cu (I)特征峰的信号强度增强,且加入BCS后Cu (I)在Cu LMM光谱中的特征峰强度明显强于添加EDTA后的特征峰强度,这与之前的实验结果一致。上述结果进一步证实了Cu (I)和Cu (II)在430-Cu SS接触杀伤中的作用。
活性氧的影响
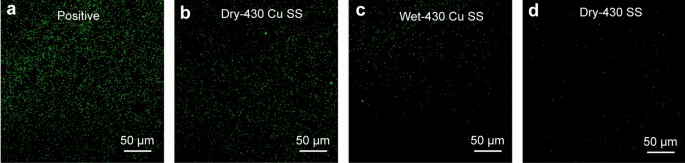
ROS作为细胞呼吸过程中氧气的代谢副产物,在维持体内稳态和细胞信号转导中起着至关重要的作用[43,44,45].但是,外部影响引起的ROS水平急剧升高,会导致细胞发生氧化应激,从而对细胞结构造成严重的、不可逆的破坏[46,47].DCFH-DA一般用于检测细胞内ROS的产生水平。如图所示。6a,阳性对照组表面出现大量绿色荧光斑,说明在Rosup试剂的刺激下,430 SS表面产生了大量ROS。数字6b, c表示大肠杆菌干法和湿法共孵育2 h后,430-Cu SS表面的绿色荧光斑明显只有湿法共孵育的430-Cu SS在激光共聚焦显微镜下才能发现少量的绿色荧光斑,说明430-Cu SS的ROS水平较低,而干法条件下430-Cu SS表面的绿色荧光斑较多,说明430- cu SS表面存在大量的ROS,并且在430 SS上几乎没有发现绿色荧光斑,ROS可能来源于呼吸链底物的末端反应[48].在有氧呼吸过程中大肠杆菌[49]时,反应底物在氧化过程中释放的电子通过呼吸链传递给氧,当接收到的电子不足时,就会形成超氧阴离子或过氧化物基团,H2O2将根据以下反应产生:
一般来说,富Cu相容易被氧化形成不同价态的Cu离子,而Cu离子不稳定,继续进行离子间转换的氧化还原反应[50],如下所示:
同时,过渡金属离子Cu (I)与H发生反应2O2在较低的毒性下通过Fenton反应生成活性极高的羟基自由基[51]:
羟基自由基具有较强的氧化性,在Fenton反应产物中起着重要的作用。因为丰富的H2O2是在有氧呼吸时产生的大肠杆菌,通过Haber-Weiss循环,根据以下两种反应,不断产生大量的高活性ROS [52]:
高活性ROS的增加具有更高的毒性作用,可刺激受体通路死亡,引起不可逆的细胞损伤甚至凋亡。因此,上述结果表明,ROS表达水平越高,接触杀灭的绝育率越高。
结论
本文从材料和生物学方面对含铜430铁素体不锈钢的抗菌机理进行了初步研究。实验结果表明,Cu含量的增加有效地提高了430-Cu SS的耐腐蚀性能和抗菌性能,并且使其之间充分接触大肠杆菌430-Cu SS表面有利于细菌的快速灭活,说明430-Cu SS的主要抑菌机制是接触杀灭,在这一过程中,有效促进了430-Cu SS基质中富Cu相的Cu离子的转化,而Cu (I)在细菌灭活中的作用比Cu (II)更重要。此外,Cu离子的价态转化产生大量ROS,影响细菌细胞代谢,导致细菌灭绝。
参考文献
- [1]
刘伟,管伟,钟宁。中国抗击新冠肺炎疫情的策略与进展。工程。2020;6(10):1076。
- [2]
郑德荣,关宇。禽流感病毒(H5N1):对人类健康的威胁。临床微生物学杂志2007;40(2):243。
- [3]
产肠毒素大肠杆菌感染。Curr infected Dis rep 2019;21(3): 9。
- [4]
肠外致病性的大肠杆菌:毒性与抗生素耐药性的结合。Microbiol前面。2012;3(9):9。
- [5]
黄海燕,李志强,李志强,李志强,李志强大肠杆菌.Microbiol Spectr。2018;6(4):289。
- [6]
铜:生物学中不可或缺的金属。咕咕叫医学杂志。2011;21 (21):R877。
- [7]
刘志强,刘志强。细胞铜分布:一种机械系统生物学方法。中国生物医学工程学报。2010;24(4):433 - 436。
- [8]
Hans M, Mathews S, Mucklich F, Solioz M.铜的理化性质对其抗菌活性的重要意义并建立了一个统一的模型。Biointerphases。2016;11(1):018902。
- [9]
张娥,傅胜,王睿,王睿,李浩,刘勇,马智,刘刚,朱超,秦刚。Cu元素在生物医用金属合金设计中的作用。罕见。2019;38:476。
- [10]
杨凯,南璐,杨凯。含铜抗菌不锈钢中Cu离子的溶解。高等学校学报(自然科学版),2010;26(10):941。
- [11]
詹智,李旭,曹勇。新型Fe-Cu复合材料的设计与性能研究。中国珍稀植物学报。2020;44(2):153。
- [12]
430型不锈钢在氯化物液滴下的点腐蚀。腐蚀科学。2010;52(6):2035。
- [13]
A.不锈钢在汽车工业中的应用。Adv Mat Res. 2013;794:731。
- [14]
王慧,肖卓,六月强,杨慧,曹卓,郭旭。烷基硅烷与氟烷基硅烷sam改性430不锈钢表面耐蚀性的比较研究。钢铁学报2013;20(12):75。
- [15]
结构用Cashell KA, Baddoo NR铁素体不锈钢。薄壁结构。2014;83:169。
- [16]
赵军,翟震,孙东,杨超,张欣,黄宁,蒋欣,杨凯。模拟生理环境下抗菌钝化316L不锈钢的抗菌耐久性及生物相容性。中国科学:地球科学。2019;
- [17]
倪慧,张慧,陈锐,詹伟,霍凯,左智。银、铜离子注入对AISI 420不锈钢的抗菌和耐腐蚀性能的影响。金属学报。2012;19(4):322。
- [18]
张欣,黄旭,勇明,林宁,范安,唐斌。含铜不锈钢表面的杀菌行为。计算机科学与技术。2012;24(4):362 - 368。
- [19]
张欣,杨超,杨凯。基于微畴电位差电荷转移的含铜不锈钢接触杀灭。ACS应用板牙接口。2020;12(1):361。
- [20]
孙松,赵安,曾强,尹浩。连续退火温度对超纯铁素体不锈钢组织和性能的影响。钢铁学报(英文版). 2017;31(7):391 - 396。
- [21]
Bartram J, Cotruvo J, Exner M, Fricker C, Glasmacher A.饮用水安全管理中的异养板计数测量:日内瓦专家会议报告,2002年4月24-25日。国际食品微生物学杂志2004;92(3):241。
- [22]
南璐,徐东,顾涛,宋旭,杨凯。微生物对304L-Cu不锈钢耐腐蚀性能的影响大肠杆菌.中国生物工程学报,2015;28(5):532。
- [23]
孙勇,杨超,杨超,徐东,李强,尹亮,邱超,刘东,杨凯,不同腐蚀微生物对X80管线钢的影响,金属学报。Sin-Engl。2019;32(12):1483。
- [24]
李敏,南玲,徐东,任刚,杨凯。含铜不锈钢对自来水微生物的抗菌性能研究。高等学校学报。2015;31(3):349。
- [25]
何志强,何志强,何志强,何志强2 +和铜+二磺酸盐配合物促进ros检测化合物二氯荧光素(DCFH)的氧化。生物化学。2006;385(5):959。
- [26]
Hicks J, Halkerston R, Silman N, Jackson K, Aylott W.基于细胞内ROS传感平台的实时细菌检测。Biosens Bioelectron。2019;141:111430。
- [27]
辛胜,李敏。316L型不锈钢在热浓缩海水中的电化学腐蚀特性。腐蚀科学。2014;81:96。
- [28]
耿鹏,赵军,席涛,杨超,杨凯。模拟生理溶液中含cu L605合金钝化膜的稳定性及抗菌性能。罕见。2020;39(1):1。
- [29]
刘勇,陈东,杨凯,王峰。铜对不锈钢电化学腐蚀和钝化行为的影响。Electrochim学报。2010;55(17):5028。
- [30]
刘旭,刘玲,隋峰,毕华,常娥,李敏。Cu对冷轧204不锈钢组织和耐蚀性的影响。固体化学学报。2020;24(1):1197。
- [31]
周娥,李慧,杨超,王军,徐冬,张冬,顾涛。海水绿脓杆菌生物膜对2304双相不锈钢的加速腐蚀。国际生物降解物学报,2018;127:1。
- [32]
李萍,赵颖,刘颖,赵颖,徐东,杨超,张涛,顾涛,杨凯,2205双相不锈钢中添加Cu对铜绿假单胞菌生物膜抗点蚀性能的影响。高分子学报。2017;33(7):723。
- [33]
刘志强,刘志强。Cr-Mn-Ni不锈钢在醋酸溶液中的腐蚀行为。腐蚀。2010;66(8):292。
- [34]
Rondelli G, Torricelli P, Fini M, Giardino R.用EIS对骨科应用的无镍不锈钢的体外腐蚀研究。生物材料,2004,26(7):739。
- [35]
王志强,王志强,李志强,等。铜对铁表面细菌的还原及接触杀灭作用。中国生物医学工程学报。2015;31(5):433 - 436。
- [36]
Mathews S, Hans M, Mucklich F, Solioz M.如果铜离子能诱导细菌与金属的接触,那么细菌对铜的接触杀灭作用就会被抑制。中国生物医学工程学报。2013;29(8):362 - 368。
- [37]
王晓明,王晓明,王晓明,等。干燥金属铜表面对细菌的杀灭作用。中国生物医学工程学报。2011;30(3):374 - 379。
- [38]
山竹C、Taudte N、Nies D、Grass g大肠杆菌在金属铜表面。环境科学与技术。2008;34(4):393 - 393。
- [39]
李志强,李志强,李志强,等。不锈钢表面单核细胞增生李斯特菌生物膜的扫描电镜观察。《兽医贝尔格莱德。2009;59(4): 423。
- [40]
刘荣,张勇,马震,任磊,杨凯,含铜钛合金(Ti-Cu)对细菌的抑菌作用变形链球菌而且Porphyromonas gingivalis.Sci众议员2016;6(1):29985。
- [41]
高德塞拉希T, Vesaghi M, Shafiekhani A, Baghizadeh A, Lameii M. XPS研究Cu@Cu2核壳纳米粒子。计算机科学与技术。2008;22(5):362 - 368。
- [42]
刘志强,刘志强,刘志强,等。CuO和Cu的表面氧化还原2O采用XPS和XAES进行研究。冲浪界面分析。1996;24(12):811。
- [43]
王志强,王志强,王志强,等。活性氧在炎症信号转导中的作用。中国保监会研究》2018;122(6):877。
- [44]
Hensley K, Robinson K, Gabbita S, Salsman S, Floyd R.活性氧,细胞信号转导和细胞损伤,自由基。生物医学杂志。2000;28(10):1456。
- [45]
氧化应激诱导肝损伤中的细胞信号转导。中华肝病杂志。2007;27(4):378。
- [46]
张志强,张志强,等。活性氧在植物细胞死亡中的作用。植物杂志。2006;141(2):384。
- [47]
氧化应激是添加糖诱导心血管疾病的机制之一。国际医学杂志。2014;23(4):217。
- [48]
尹珊珊,吴浩,李珊珊,刘洋。细胞信号转导中活性氧生成的调控。摩尔细胞。2011;32(6):491。
- [49]
张志强,张志强,张志强,张志强2O2自由基诱导内皮细胞氧化应激。生物医学。2006;40(12):2206。
- [50]
张志强,张志强。金属离子自由基的氧化机理研究。生物医学。1995;18(2):321。
- [51]
孙燕,田鹏,丁东,杨智,韩宇。cu基非均相芬顿反应催化剂活性种类的揭示。环境科学。2019;258:117985。
- [52]
70年后的哈伯-魏斯周期。氧化还原众议员2001;6(4):229。
确认
国家重点研发计划(No. 2016YFB0300205)和中国科学院青年创新促进会(No. 2018221)资助。
作者信息
从属关系
相应的作者
权利和权限
关于这篇文章
引用这篇文章
张忠,张晓荣。,金,T。et al。含铜430铁素体不锈钢的抗菌机理研究。罕见的了。(2021)。https://doi.org/10.1007/s12598-021-01751-y
收到了:
修改后的:
接受:
发表:
关键字
- 铜不锈钢
- 耐蚀性
- 抗菌机制
- 接触造成
- 铜离子。
- 活性氧(ROS)